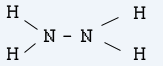В „Мемоари“ („Memoirs“) на Академията на науките на Санкт Петербург от 1810 г. известният историк на науката Юлиус Клапрот (1783 – 1835) превежда „Признанията на мирния дракон“ на Мао Хуа – книга, донесена наскоро от Китай от френски пътешественик. В тази книга, датираща от 756 г. след Хр. (от времето на династията Тан), Хуа нарича кислорода „чи йин“ и обяснява, че макар той да не се среща никъде в чиста форма, се намира във въздуха. При горене се свързва с други елементи, включително метали, и образува нови вещества. Книгата добавя, че кислородът е една от съставките на водата. Ако Мао Хуа е открил кислорода през VIII век, това е постижение, което заслужава голяма слава. За съжаление няма следа от него, нито от неговата книга с изключение на работата на Клапрот. Ако Клапрот е сбъркал в датировката, може да се предположи, че Мирният дракон е направил тези признания, след като английският теолог Джоузеф Пристли (1733 – 1804) е открил кислорода. През 1774 г. Пристли публикувал по-пълно от това на Мао Хуа описание на кислорода. Ако всички участници са се движели бързо, откритието на Пристли може да е пренесено в Китай и обяснено на Мао Хуа, записано в един или няколко екземпляра, един от които случайно попаднал на французин, посетил Китай, който от своя страна го оставил в Русия навреме, за да успее Клапрот да подготви своята публикация от 1810 г. Такава верига от събития, макар все пак да е възможна, не може да обясни годината 756, цитирана от Клапрот. Мао Хуа, или който и да е този, който му е разказал за кислорода, остава една от най-загадъчните личности в историята на науката. Ако това се окаже фалшификат, тогава заслугата за първото откритие не е на Пристли, а на шведа Карл Шееле, който открил кислорода през 1772 или 1773 г. и публикувал своето откритие през 1779 г.
Михаил Василевич Ломоносов

Епохата, в която се ражда и твори Михаил Василевич Ломоноеов, е епоха на бурно икономическо и културно развитие на феодално-крепостна Русия. Амбицията на Петър Велики да изведе Русия на едно от първите места между европейските държави довежда до развитието на манифактурата, корабостроенето, металургията и търговията, за които са необходими специалисти от всички области на науката и техниката. Създават се специални училища и необходимата за тях литература, а в 1724 г. в Петербург е основана Руската академия на науките, в която по-късно учи и работи Ломоносов.
Суровата природа на беломорския север, където живеят будни и предприемчиви хора, непознали татарското робство, помещичесхото земевладение, оказва извънредно благотворно влияние при формиране характера на Ломоносов, а културният и обществено-икономическият подем на Русия — върху творчеството му.
Още 10-годишен Михаил придружава баща си в пътуванията му из Бяло и Баренцово море, наблюдава многобройните и интересни явления на северната природа и натрупва много познания по морското дело и риболова. На 14 години пише без грешки и селяните го търсят за написването на необходимите им документи. Но освен граматиката на Смотрицки и аритметиката на Магнитски в родното място се намират само религиозни книги. В края на 1730 година Ломоносов избягва от къщи и се отправя пеш към Москва, за да изучава латински език, на който, по думите на учителя му Шубин, са написани най-хубавите книги.
Първоначално в Цифирната школа, а по-късно в Славяногръко-латинската академия Ломоносов изучава основно латински и гръцки език, чете в оригинал съчиненията на старите гръцки и римски мислители, сам написва твърде голям курс по риторика и прави първите си стихотворни опити. Неизяснени остават най-интересните за него въпроси — естественонаучните. В края на 1735 год. идва заповед на Сената в Петербург да се изпратят десетина от най-будните младежи на Спаските училища да продължат обучението си в Петербургската академия. Между избраниците е и безкрайно щастливият Ломоносов. Тук обучението се води по нова програма лекциите са на по-високо ниво, изучава се математика, риторика, история, география, латински и немски език и танци. Интересни лекции по физика чете академик Крафт, провеждайки опити с нови и съвършени за времето си апарати.
По същото време Академията организира голяма експедиция за изучаване на Сибир, за която е необходим химик, запознат и с минното дело. Тъй като такъв човек в Академията няма, ръководството решава да изпрати за подготовка в Германия трима студенти — Райзер, Виноградов и Ломоносов.
Марбургският университет, в който постъпват тримата младежи, е един от най-старите в Германия и първият основан без помощта на папата, поради което, се ползва с по-голяма свобода. Централна фигура е Хр. Волф, който въпреки идеалистическите си схващания е добър преподавател, а университетската библиотека разполага със съчиненията на Галилей, Торичели, Мариот, Хюйгенс, Декарт, Бойл и др. Под ръководството на Волф Ломоносов подготвя и изпраща в Петербург две самостоятелни работи „За превръщането на твърдите тела в течни“ и „Физическа дисертация за различията между смесените тела, състоящи се в сцепление на корпускулите“. В тях изяснява свойствата на телата от собствена материалистическа позиция.
– Вторият период от престоя в Германия във Фрайберг при Хенкел, който, по думите на Ломоносов, „презира всяка разумна философия“, е период на интензивна самостоятелна работа и наблюдение в рудниците. Тях по-късно оформя в съчинението „Върху земните слоеве“. Освен това работи върху руския стих и неговите особености. Поради изострени отношения с Хенкел Ломоносов напуска тайно града, отива в Маргбург, оженва се за дъщерята на скромен пивовар, но не остава дълго при немското семейство, а се отправя към Амстердам и търси кораб за Русия. По пътя се среща с видния холандски металург и химик Крамер и известно време работи в химическата му лаборатория. В Дюселдорф става жертва на измама и е вербуван за войник на пруския крал, но успяза да избяга, което прави престоя му в Германия невъзможен, и през юни 1741 г. се завръща в родината.
В Петербургската академия на науките Ломоносов постъпва първоначално като специалист, а от 1.1.1742 г. е назначен за асистент по физика. По това време в Академията господстващо влияние имат чужденците начело с Шумахер, които пречат на самостоятелното развитие на руската наука и култура. Още първите години Ломоносов повежда борба срещу чуждото влияние, за което е изключен от състава на Академията и дори престоява шест месеца в затвора. Разбирайки, че за да прокара своите идеи, трябва първо да се стабилизира, Ломоносов подава молба за присъждане на професорско звание и през юли 1745 г. е избран за професор по химия. Въпреки избора Шумахер изпраща научните му трудове за рецензия на Ойлер. Получава се извънредно ласкав отзив. Оттогава между двамата учени се поражда дружба, която продължава до смъртта на Ломоносов.
През първия период на своята дейност Ломоносов провежда предимно физически изследвания—до 1748 г., когато успява да издействува създаването на химическа лаборатория и поставя основите на руската химия. Като учен-енциклопедист до края на живота си работи в най-различни области на науката: развива корпускулярната теория, в която въвежда понятията „корпускула“ и „елемент“, извънредно много приближаващи се до съвременната молекула и атом; разглеждайки материя и движение в неразривна връзка, дефинира закона за запазване на веществото и движението; отхвърля теорията за топлорода и обяснява топлината чрез движението на корпускулите; разглеждайки химията в неразривна връзка с физиката и математиката, поставя основите на физикохимията като наука; провежда редица изследвания в областта на електричеството, метеорологията, геологията, минното дело, металургията, географията и историята; разработва конструкцията на оптични уреди, инструменти и редица въпроси из областта на теоретичната оптика; открива наличието на атмосфера на Венера. В областта на литературата и изкуството Ломоносов има заслуги за чистотата на руския език и звучността на стиха, разглежда редица стилистични и граматични въпроси за преобразуване на руския език, въвежда нови понятия и думи, научна терминология, сам пише стихове. Не случайно сто години по-късно Белински го нарича „Петър Велики на руската литература“.
За една от главните задачи на своята научна и просветителска дейност Ломоносов смята повишаването на културата на руския народ, от чиито недра ще израснат бъдещите нютоновци и платоновци. През целия си живот той се бори за създаване на демократически университет и успява в това си начинание. Като началник на академичната канцелария раздвижва редица въпроси във връзка с научната подготовка на студентите, увеличението броя на печатните книги и др., популяризира своите естественонаучни разбирания и се бори за изграждане на правилен естественонаучен мироглед. Тази широка дейност му спечелва много врагове, особено между духовенството, които по времето на Екатерина II взимат връх. Почива на 15.IV. 1765г. самотен, но непримирен, все още с много идеи за бъдещето на руската литература и Академията. Погребан е в лаврата Александър Невски.
П. Ачкова
Източник: nauka.bg
Състав на въздуха
 Кавендиш е изследвал и обикновения въздух, за да определи състава на атмосферата. Карл Шееле (1742 – 1786), един от откривателите на кислорода и азота, вече е определил, че въздухът е смес от двата елемента. Кавендиш е установил, че пропорцията е 20,83 % кислород и 79,17 % азот, като всичко друго се смята за примеси.
Кавендиш е изследвал и обикновения въздух, за да определи състава на атмосферата. Карл Шееле (1742 – 1786), един от откривателите на кислорода и азота, вече е определил, че въздухът е смес от двата елемента. Кавендиш е установил, че пропорцията е 20,83 % кислород и 79,17 % азот, като всичко друго се смята за примеси.
Откриване на водорода
Водородът е открит през 1766 г. от състоятелния класически учен Хенри Кавендиш (1731 – 1810) в неговата частна лаборатория в Лондон. Той го кръстил „избухлив въздух“ заради това, което се случва, когато към него се поднесе огън. През 1781 г. Кавендиш открил, че може изкуствено да създаде вода, когато взриви заедно водород и обикновен въздух. По-късно повторил експеримента с водород и кислород и успял да изчисли, че водата е съставена от тези два елемента и да определи пропорциите на всеки от тях в нейния състав.
Афинитет на елементите
Шведският химик Йонс Якоб Берцелиус (1779 – 1848) е съставил първата таблица на елементите, в която всеки елемент е подреден в съответствие със силата на неговия положителен или отрицателен електрическа заряд. Той е открил, че големината на афинитета между два елемента е пропорционална на разстоянието на което са разделени те в неговата таблица.
Лизозоми (lisosomata)
Oткрити са от К. де Дюв в началото на 50-те год. На 20 век.
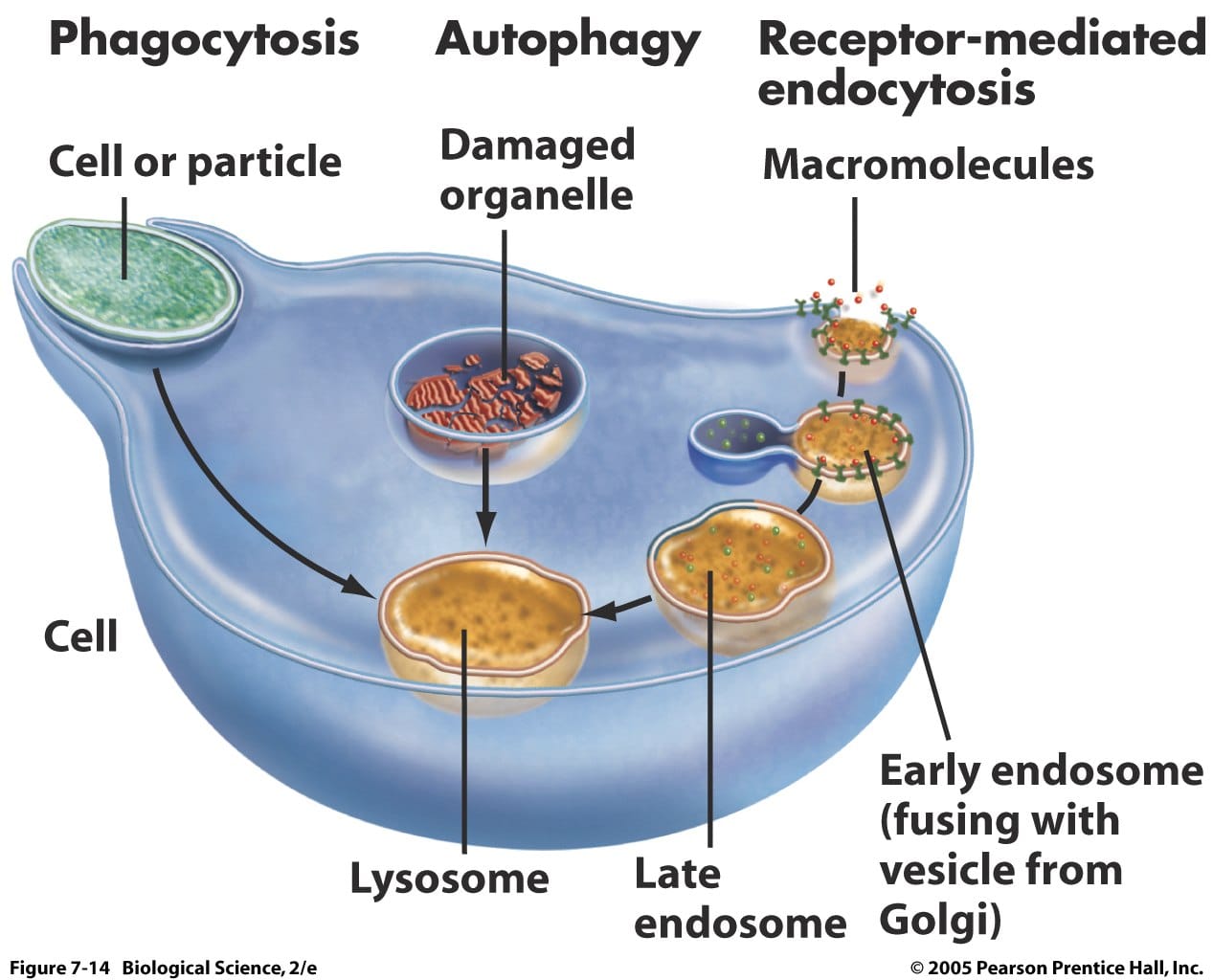
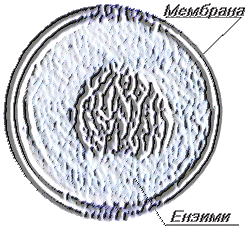
Лизозомите са органиоди и на вътрешната мембранна система на клетката, изпълняваща литични функции те участват в смилането на екзогенните вещества и в елиминирането на отделни вътреклетъчни части (автофагия). Имат кълбовидна, яйцевидна форма и големина от 0,1 до 0,8 µm. Изградени са от гранулирана елекртонноплътна маса, наречена матрикс обграден от двуслойна мембрана, която за разлика от митохондриалната не образува кристи.
Гранулираната вътрешност на йизозомите съдържа голям брой хидролитични ензими, между които значително място заема киселата – фосфатаза, която се смята като маркер на лизозомите. Лизозомите съдържат и други ензими – нуклеази, фосфопротеинфосфатаза и др. Количеството на хидролазите в лизозомите е огромно.
Лизозомите извършват и м-са на апоптолиза – самоунищожение на клетките.
Лизозомите се подразделят на първични и вторични.
Първични лизозоми – Те са изградени от финно гранулиран плътен матрикс. Образуват се от периферните издути части на цистерните на апарата на Голджи. Първичните лозозоми не са активни, защото се съдържат събстрат ( чужд белтък, бактерии и др.)
Вторичните лизозоми са ативни, затова в тях често се срещат полъсмлени или неразтворени остатъци от чужди вещества или собствени вещества от метаболизма на клтката. Вторичните лизозоми се подразделят на :
- Смилателни вакуоли
- Автолизозоми
- Щитоергозоми
- Мултивезикуларни телца
- Телозомни ( остатъчни телца)
Лизозома
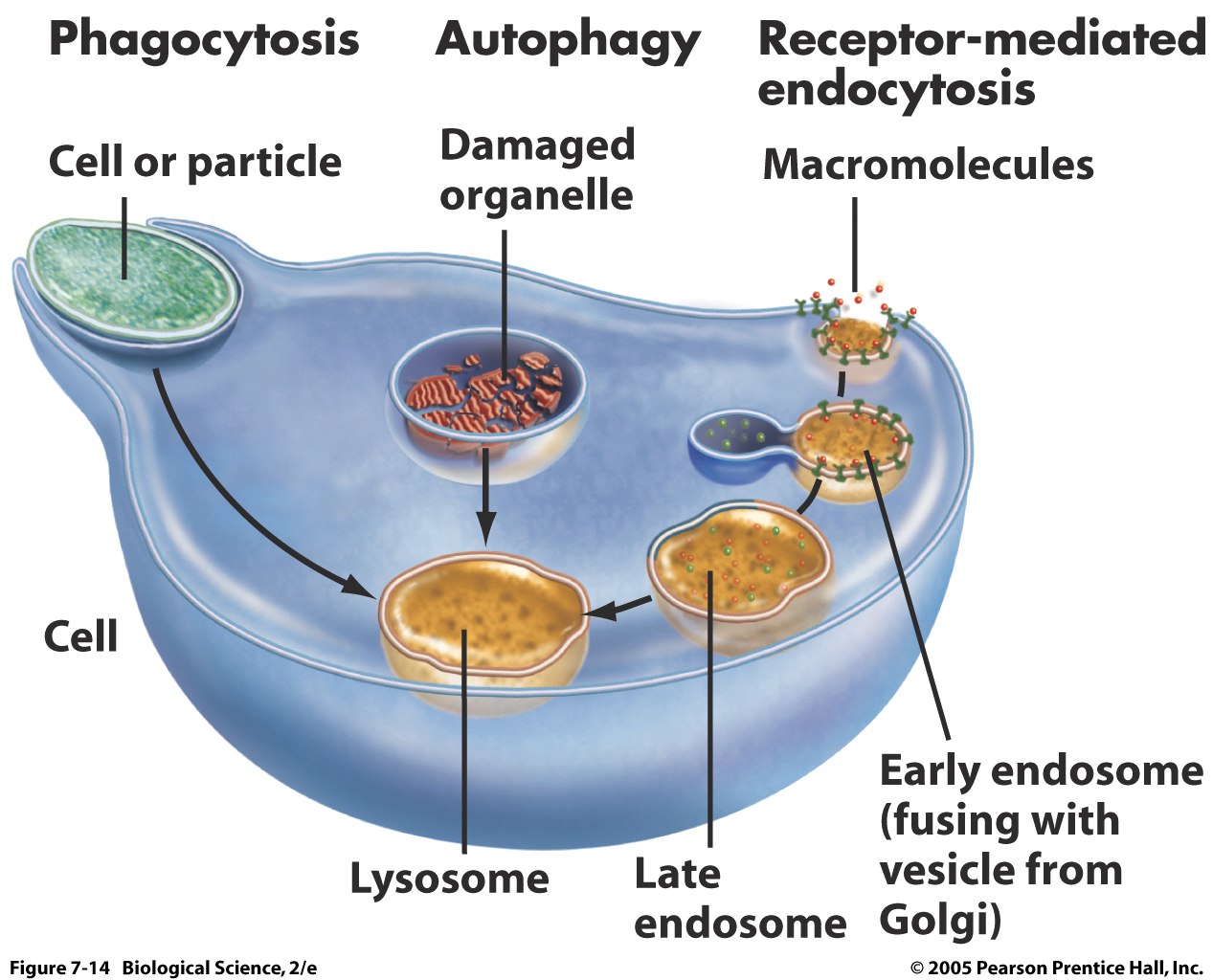
ФУНКЦИЯ НА ЛИЗОЗОМИТЕ
Когато „остареят”, част от част от органелите на клетката (митохондрии, едноплазмен ретикулум и др.) се елиминират, като първоначално се ограждат от каналчета на едноплазмения ретикулум, изпълнени смного хидролитични ензими. Тези каналчета, съсдържат хурдрол. зими и огадените цитоплазмени органели образуват автофагозома. Това явление се нарича автофагия. Към тези тени автоагозоми се присъединяват първичните лизозоми и автофагозомите се превръщат в автолизозоми (цитолизозоми). Когато автолизозомите се слеят образуват цитосегрозоми. Когато съдържанието в автолизозомите, респективно в цитосегрезомите се разгради под действието на хидролит. ензими (и след като част пт смлените вещества се използват от клетката ) остават крайни образувания – телолизоми. Веществата от, които се изхвърлят от клетката след преработка.
Лизозомите (автолизозомите и цитосегрезомите) извършват и автолиз (според някой автори понятието е апоптоза) на клетката, ако тя е увредена.
Лизозомите имат и друга функция – модигикация на клетъчни продукти. Наример в клетките на штитпжидната жлеза едноплазмения ретикулум синтезира тироглобулин (белтък предшественик на тиропния хормон) След секрецията на тироглубина от едноплазмения ретикулум, последния се слива с първичните лизозоми, хидлолитичните ензими на които го трансформират в тироиден хормон, който след това се извежда в кръвния поток.
Според съвременните представи лизозомния апарат се е развил като специализирана част на катаболитната система на цитоплазмата с широка функционална пластичност.
ПЕРОКСИЗОМИ
Рази група микро телца е наречена пероксизоми от К. Де Дзв през 1956 г. Те са неголеми вакуоли, обвити с единична мембрана, ограничаваща рганулирания матрикс. В центъра на матрикса има сърцевина. В зоната на сърцевината се намира паракристална структура, състояща се от подредено опаковани фибрили и тръбици.
Пероксизомите са открити при протисти (амеби), при низити гъби (дрожди), при висши растения (ембрионални тъкани, ендосперм), при висши гръбначни животни, главно в черния дроб и бъбреците.
(щракнете изображението, за да го увеличите)
Комплекс на Голджи
Колмплекса на Голджи е описан през 1898 г. от Камило Голджи. Той го е наблюдавал като мрежест венец около ядрото на нервни клетки.
Обикновено той се намира до ядрото на клетката или около него. Това е свързано с основната му функция – секреторна. Възможно е и промяна на локализацията му в някой клетки във връзка с физиологичните особености на клетката.
Комплекса на Голджи съществува в три нива на организация:
- ЦИСТЕРНА – Сплесната мембранна торбичка с централно плочковидна част и перфорирана периферна зона.
- ДИКЦИОЗОМА – Група от цистери (4-8), наредени в пакет.
- Комплекс на Голджи – Няколко свързани диктиозоми. Броят им варира във връзка с физиологичните потребности на клетката.
Основна структурна единица на комплекса.
Дикциозомата е съставена от плътно разположени една до друга плоски мембранни цистерни, между които има тънък слой цитоплазма. Освен цистерните в зоната на дикциозомата се наблюдават множество вакуоли
АПАРАТ НА ГОЛДЖИ
Комплека на Голджи е полрна структура. Прието е да се различават проксимален (близък, цис) и дистален (далечен – транс) ползси. В секретиращите клетки проксималния край на комплекса е обърнат към ядрото (или едноплазмения ретикумум), а дисталния край към клетъчната мембрана (плазмената). Към проксималния полюс към цистерните на комплекса се доближават малки вакуоли (транзитни) – (транзитните вакуоли идват от едноплазмения ретикулум), а в дисталния край характерзиращи се с по-едрите разширения на цистерните, се образуват големите бакуоли съдържащи продукта на клетъчната секреция ( образувани от комплекса на Голджи)
В клетките отделните дикциозоми магат да бъдат свързани чрез система от цистерни и вакуоли.
Така се формира тримерна мрежа.
! Някой автори вместо понятието дикЦиозома използват понятието дикТиозома.
ФУНКЦИИ НА АПАРАТА НА ГОЛДЖИ !
Апарата на Голджи участва в натрупването и секресията на продуктите синтезирани в едноплазмения ретикулум, участва в тяхното химическо преустройство и узряване, полимеризация на полизахариди и образуване на комплекси от полизахариди (ПЗ) и белтъци (Б) – гликопротеиди; атно на комплекса му липиди(Л) и Б -липопротеиди и др. Освен тези вещества апарата на Голджи натрупва и други вещества – ензими, хормони, vit. Прието е, че в апарата на Голджи се извършва адсорбиране, кондензиране и опаковане на веществата, които се синтезират в гранулирания еноплазмен ретикулум и постъпват чрез транспортни вакуоли в апарата на Голджи. В апарата на голджи се формират и опаковат лизозомите и преоксизомите.
Комплекса на Голджи присъства във всички клетки на еукатиотните организми ( с изключение на еритроцитите при млекопитаещите организми), но не всяка клетка притежава способност за секреция на белтъци, Л и ПЗ (мускулни клетки, еритроцити, покривен епител). Всички те обаче притежават добре развити комплекс на Голджи. Това е свързано с образуването на лизозомите.
НЯКОЙ СПЕЦИФИЧНИ ФОРМИ НА АПАРАТА НА ГОЛДЖИ
ПРИ РАСТИТЕЛНА КЛЕТКА междуклетъчната пластинка, разделяща двете нови, дъщерни клетки след приключване на кариокинезата (делене на ядрото), се обр. от апарата на Голджи. Междуклетъчния плас е продукт на вакуоли от комплекса на Голджи, които изливат съдържанието си в екваториалната плоскост (пектин и хемуцекулата) на делящата се клетка.
Междуклетъчната пластина е изградена от пектин и хемицелулоза.
РАЗВИТИЕ НА АКРОЗОМАТА ПРИ ПРЕРМАТОЗОИДИРЕ
АКРОЗОМАТА Е МЕМБРАННА СТРУКТУРА на сперматозоида, с която той разпознава и свързва сперматозоида към повърхността на яйцеклетката.
Аузиращите от апарата на Голджи вакуоли увеличават повърхността на акрозомата.
(щракнете изображението, за да го увеличите)
Митохондрии
Митохондриите се срещат във всички растителни и животински клетки. Изкючение са едноклетъчните рукариотни организми, живеещи постоянно в анаеробна среда, дифинитивните еритроцити, в роговелите епителни клетки, мутантни дрожди, загубили изцяло или частично митохондрииния си геном. Митохондриите има собствена ДНК и се възпроизвеждат независимо от ядребата ДНК. Наблюденията на митохондриите датират от края на 20в като им са давани различни имена свързани с формата им (митозоми, хондриозоми, биобласти и да. ) В 1898 г. Бехда въвежда името митохондрии, а през 1900 г. Михаелис предлага използването на багрилото. Янус гриин Б, специфично багрещо митохондриите (хистохимичен маркер)
ФОРМА – варира силно дори в пределите на една клетка – специфичниелипсовидни, бъбрековидни, силно източени – нишководни.
РАЗМЕРИ – Дебилината на митохондриите е относително потоянна около 0,5 мкм. Дължината им се коледае от 0,5 до 7-10 мкм при хишководните (силно източените) форми.
Количеството на митохондриите в клетката е различно в зависимост от функцията на клетките.
БРОЯ на митохондриите в клетката зависи от нуждите на самата клетка от енергия и АТФ.
ЛОКАЛИЗАЦИЯТА на митохондриите също е различна, обикновено те се разполагат в тази част на клетката, където има нужда от енергия и АТФ. При недиферинциралихондриите са клетки митохондиите са разположени равномерно в цитоплазмата, а при диферинцираните като например мускулни, митохондриите се намират в близост миофибрилите; в сперматозоидите – завити са като спирала около камшичето и т.н.
СТРУКТУРА
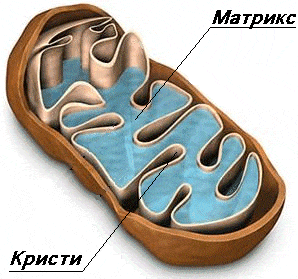
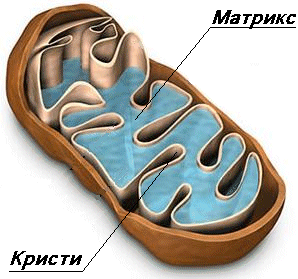
Класическите митохондрии се представят като елипсовидни органоиди, ограничени с две мембрани (двумембранни органоиди), които ги разделят на две пространства – интермембранно пространство и вътрешен матрикс.
Вътрешна митохондриална мембрана – дебелината около 7 nm – отделя съдържанието на органоида от цитоплазмата ( хиалоплазмата). Тя нормално има гладък контур и не е свързано с други мембрани в цитоплазмата притежава неспецифична проницаемост. По статична е, с белтъчно съдържание около 20%. Съдержа порови белтъци – порини през които могат да преминат всички молекули до 5000 D. Други белтъци в тази мембрана включват ензими, свързни с митохондриалния липиден синтез.
Интермрдиарното пространство е изпълнено с хомогенно течно вещвство със слаба електронна плътност. Съдържа предимно нискомолекулни съединения – кофактори и субстрати на биологичното окисление.
Вътрешна митохондриална мембрана – ограничава матрикса (митоплазмата). Тя образува многобройни вгъвания, наречени крисити. Тези нагъвания
(инвагинации) многократно увеличават повърхността на вътрешната мембрана. Криситите са насочени навътре към марикса Вътрешната мембрана се различава от външната. Тя е с висико специфинчна проницаемост, тя е по-гъвкава и по-динамична, с белтъчно съдържание 75%. Това е свързано с електрохимичния градиент на Н , който стимулира АТФ синтезата. Най-общо белтъците на вътрешната мембрана изпълняват три типа функции:
- Узвършват окислителноредукционните реакции в електрон-транспортната верига.
- Синтезират АТФ в матрикса, чрез АТФ – синтези в мембраните.
- Позволяват преминаването на метаболити навън и навътре от матрикса, чрез транспортни белтъци.
МАТРИСК
Висико концентрирана смес от стотици ензими, включително и ензими необходими за цикъла на Кребс. Матриксса има финнозърнест и хомогенен строеж. В него се наблюдават тънки нишки и гранули. Нишките са няколко копия на молекули ДНК а гранулите – митохондриални рибозоми. В матрикса се срещат по-големи гранули които са депо за отлагане на калциеви и магнезиеви соли.
МИТИХОНДРИАЛНА ДНК
Респликацията на митохондриалната ДНК протича независимо от репликацията на ядрената ДНК. Обикновенно репликацията на митохондриалната ДНК става след завършване репликацията на ядрената ДНК. Митохондриалната ДНК е двуверижна, за нея е характерна суперспирализация но има атсъствие на белтъци (при ядрената имаме хистолин). Тя обикновенно се прикрепва вътрешната митохондриална мембрана, т.е за митохондриите с характерна автономия при възпроизвеждането, но по отношение на пълна автономност относно синтезата на пълния набор от белтъци необходими за изпълнение на изпълнение на функиите си, митохондриите често използват белтъци синтезирани от цитоплазмените рибозоми, които постъпват в матрикса и се локализират на специфичните на тях
места.
ФУНКЦИИ НА МИТОХОНДРИИТЕ
- В тях се извършва цикъла на Кребс
- Окислително-фосфолиране ( синтез на АТФ )
- Бета – окисление на мастни киселини
- Елонгиране ( удилжаване ) на мастни киселини
- В митохондриите се отстраняват някой токсични събстанции.
Митохондриите са сързани главно с енергитичния метаболизъм на еукариотната клетка клетката – синтез на АТФ. Стратегията на цикъла на Кребс е същата с тази на гликозата ( извършва не при анаеробни условия в цитоплазмата),а именно: Разграждане на голени въглеводородни молекули с отделяне на енергия по формата на АТФ или под формата на НАДН2 и ФАДН2
ОКИСЛИТЕЛНО – ФОСФОРИЛИРАНЕ – Водорода от НАДН2 и ФАДН2 се подава по веригата от най-малко пет междинни субстанции [Тази верига се нарича електрон-транспортна верига (дихателна верига)]. Този водород по тази верига достига до молекулата на О2 и се образува Н2О. Всяко пренасяне на Н редуцира (приема е-) на донорната молекула.
Преноса на Н в началото на веригата, а в края на е- създават електроден градиент който е причина за фосфолиринато на АДФ до АТФ. В този процес участват оксизолите в чиито главички е разположен АТФ – цинтетазния комплекс
Я-ОКИСЛЕНИЕ – Свободни мастни киселини се отркиват в клетката само в следи, защото са силно токсични. В цитоплазмата масните кислелини се свързват с глицерол в моноди и триглицериди и фосфолипиди. Те се хидлолизират в цитокл. и се транспортират в митохондриите кдето се окисляват напълно
(Я-ОКИСЛЕНИЕ )
ЕЛОНГОРАНЕ НА МАСТНИ КИСЕЛИНИ – Най-общо мастните киселини се синтезират в агранулирания едноплазмен ретикулум но в митохондриите също има ензими катализаращи елонгирането на палмитинова и др. наситени мастни киселини.
Хидразин
Частично окисление на амоняк (NH3) води до получаване на хидразин.
2NH3 NaOCl –> N2H4 H2O NaOH
Хидразинът представлява безцветна, димяща на въздуха течност (т.т. 1,4°С ; т.к. 113,5°С )
Хидразинът и водните му разтвори се използват като редуктори при което се окислява до азот.
HO2 CH3N2H2 –>
Анализ на месинг
Количественото определяне на съставките на сплавите заема значителен дял от приложния анализ. То е от голямо значение за металургията и за металознанието.
Анализът на месинг е един от най-характерните анализи на сплави. Както е известно, съставът на месинговата сплав включва Cu в преобладаващата част, Zn също в значително количество, а в малки количества— от следи до 1—2% — Pb, Sn и Fe.
Пробата се подготвя под формата на стружки. За изходно количество се взема около 0,5 g и се претегля с точност до четвъртия знак. За разтварянето й е достатъчно да се залее в бехерова чаша с вместимост от 150 до 200 cm3 с около 10 cm3 разр. HNO3(2 : 1). Буйно протичащата реакция води до опасност от изпръскване. Ето защо чашата се покрива с часовниково стъкло. Ако останат не разпаднати стружки, чашата леко се нагрява. Доба вят се 60 cm3 дестилирана вода, нагрята до кипене, и внимателно се смиват стените на чашата с пръскалката, като пръските от получавания разтвор се задържат от покриващото часовниково стъкло. За да приключи реакцията, необходимо е допълнително леко нагряване в продължение наполовин час. При обработването на сплавта с HNO3 калаят преминава в метакалаена киселина:
3Sn 4HNO3 H2O –>ЗH2SnO3 4NO.
Тя пада като утайка, филтрува се през плътен количествен филтър (предпочита се синя лента). За да се освободи утайката от разтворимите примеси, промива се с гореща вода. В нея предварително се разтваря малко количество от летливия електролит NH4NO3.
Промитата утайка се суши при 118°С. След това се нагрява в плитък порцеланов тигел, като се осигуряват окислителни условия на накаляването. Протича следната реакция:
H2SnO3=SnO2 H2 O
Когато се достигне постоянна маса, утайката се тегли като SNO2 и се изчислява в проценти спрямо изходната маса на пробата.
Следващият метал, който се отлъчва, е Pb. Когато се прилага тегловният метод, за подходяща форма на утаяване се избира PbSO4. Намиращият се във филтрата Pb(NO) 3) 2 се превръща в PbSO4, като се действува със H2SO4:
Pb(NO3)2 H2SO4=PbSO4 2HNO3
Тъй като NO3 силно влияе на разтворимостта на PbSO4, за да не се компрометира резултатът, налага се HNO3 изцяло да се отстрани от филтрата. За целта към него се добавят 4 cm3 конц. H2SO4 и се изпарява в порцеланово блюдо, докато започнат да се отделят гъсти пари от SO3– Препоръчва се поне веднаж да се прекъсне нагряването, за да се свалят със струйка вода отложените по стените на блюдото соли.
Когато изпаряването привърши, остатъкът в блюдото се залива с 25 cm3 студена вода. Получената кора от соли се раздробява със стъклена пръчка. Подлага се отново на нагряване до кипване. С това се цели да се отделят разтворимите във вода сулфати от кристалите на утайката на PbSO4. Доливат се отново 50 cm3 вода и след като утайката се охлади в продължение на един час, се филтрува през предварително изсушен и претеглен филтър-тигел. Филтруваната утайка първоначално се промива с разредена H2SO4, а след това с алкохол. С това по-пълно се ограничава разтворимостта на PbSO4 в промивайте води. Промитият филтър-тигел се суши при 200° С до постоянна маса.
Определянето на Pb може да се извърши и ускорено но електроана-литиченпът. Това обаче е свързано с употребата на скъпи платинови електроди.
Третият метал, който се отлъчва, е медта. Във филтрата, получен от отделянето на PbSO4, той се намира като CuSO4 и може да се определи както тегловно, така и електроаналитично.
При тегловното определяне се спазва следната последователност.
Филтратът се концентрира на водна баня в порцеланово блюдо до обем от около 150 cm3. Прехвърля се количествено в конична колба. Добавят се 15 cm3 конц. H2SO4. Когато температурата му спадне на 70°С, през него се пропуска бавно струя от чист H2S. Получената утайка трябва да се филтрува незабавно поради опасността от окисляването на CuS до CuSO4 под действието на атмосферния кислород. Използува се смукално шише е филтър бяла лента. Измива се с 4%-ен разтвор на оцетна киселина, наситена със H2S. С това се предотвратява пептизацията на утайката от CuS. Едно от важните изисквания както при филтруването, така и при промиването е филтърът да бъде винаги запълнен с разтвор. С това се препятства окислителното действие на атмосферата, в резултат, на което CuS частично преминава в разтворимия CuSO4.
Утайката се суши, след което се отделя количествено от филтъра върхубяла гланцова хартия. Така обработеният филтър се изгаря в предварително накален и претеглен тигел на Розе. След това се прибавя и утайката. Накаляването се извършва за късо време при достатъчен достъпна въздух. По този начин филтърните влакна, увлечени в утайката, изгарят на-пълно. След като утайката се охлади до стайна температура, в тигела се насипва химически чиста сяра така, че да покрие утайката. Поставя се и капакът и неговата луличка се свързва с Киповия апарат. Произвежданият в него водород предварително се прекарва през промивно шише, съдържащо алкализиран разтвор от KMnO4. Целта е да се задържат минималните количества арсеноводород, които се отделят при получаването на водород в Киповия апарат. Присъствието му в тигела би повлияло на точността на резултата.
След като водородната струя изпъди въздуха от тигела на Розе, неговото дъно се нагрява с горелка до слабо червена жар. При това сярата, която сублимира, и водородът се запалват на изхода на тигела. Създадените условия, както лесно можем да се убедим, не допускат утайката от CuS да се окисли до CuSO4. След нагряване от 10 min при усилена струя се спира горелката. Подаването на H2 спира след още 2—3 min. Тигелът се темперира в ексикатор и претегля. След това нагряването при описаните условия продължава, докато се получи постоянна маса.
Утайката е под формата на Cu2Sпоради излишъка от химически чиста S, с която се обработва филтруваната утайка от CuS. Ето защо при изчисленията се взима под внимание този факт.
Значително по-лесно се извършва електро аналитичното определяне. Филтратът се концентрира до около 100 cm3. Към него се добавя 1 cm3 конц. HNO3 и се електро анализира.
Предпоследният метал от сплавта, който се отлъчва, е желязото. Неговото определяне се извършва по познатия тегловен начин, и то направо катоFe(OH) 3, ако преди това медта е отлъчена електро аналитично. Ако е следван тегловният метод за определяне на медта като Cu2S, се извършва следната предварителна обработка на филтрата. Отстранява се съдържащият се в него H2S (останал от насищането при предишното отлъчване). Това се постига с продължително нагряване на филтрата. В противен случай Н28 предизвиква примесване в утайката и на FeS, което понижава точността на резултата.
За да може Fe3 да паднат като утайка от Fe(OH) 3, предварително се окисляват с 2—3 капки бромна вода или конц. HNO3. Следва утаяване с 2n NH3. Разликата от познатия тегловен метод за определяне на Ре е. в употребата на значителен излишък от NH3. С това се предотвратява съвместното утаяване и на Zn като Zn(OH) 2. В останалия си ход определението следва познатия начин на работа.
Последният метал в месинга, който трябва да се отлъчи, е Zn. Филтратътс промивните води от предишното определение се изпарява до сухо в порцеланово блюдо, което се загрява на водна баня. За да се отстрани нежеланият излишък от летливите амониеви соли, остатъкът върху блюдото се накалява леко. След това се разтваря във вода, подкиселена слабо съсHCl. От така подготвения разтвор Zn2 -йони се утаяват като ZnNH4PO4. Това се постига, като средата предварително се неутрализира с NH3.За неутралната точка се следи с няколко капки от индикатора метилрот. След като разтворът се нагрее до кипване, прибавят се 20 cm3 20%-ен разтвор от (NH4)2HPO4. Той трябва да бъде прясно приготвен. За да могат да се превърнат наличните Zn2 йони изцяло, в добре кристализиращия ZnNH4PO4,кипенето продължава върху водна баня в продължение на половин час.Внимава се утаяването да не се извършва в кисела среда. Ето защо не трябва да се променя жълтият цвят на индикатора метилрот. За да може кристалната утайка да узрее добре, изчаква се около един час. Филтрувасе през количествен филтър бяла лента. Поради склонността на Cl– -йони, да се задържат в кристалите на ZnNH4PO4 утайката се промива 1%-ен разтвор на утаителя. Когато в промивните води се констатира с помощта на AgNO3 отсъствието на Cl– -йони, промиването продължава с 50%-ен алкохолен разтвор. Така се отстранява нереагиралият (HN4)2HPO4.
Промитата утайка се суши.. Снема се от филтъра върху черна гланцова хартия. Филтърът се изгаря в предварително накален и претеглен тигел. Съвместното изгаряне и накаляване на утайката с филтъра може да доведат до включване в получаваните кристали от Zn2Р2О7 на недоизгорели въглеродни частици. А това не позволява тяхното отстранявана при температура на накаляването и намалява точността на резултата.
След като филтърът се изгори в тигела, прибавя се количествено и утайката и се подлага на накаляване до постоянна маса. Утайката се превръща, в Zn2P2О7 по уравнението
2ZnNH4РО4==Zn2 Р2О7 2NHз Н2О
На тази стехиометрична основа се изчислява съдържанието на Zn в месинга.
Като ориентировъчни за правилността на резултата от анализа могат да служат следните гранични, стойности, с които отделните метали участвуват в състава на различните видове месинг: Sn—0 до 1%; Pb—-от 0до 2%; Cu—от 55 до 72%; Fe—от 0 до 1%; 2п—от 25 до 45%.



 Кавендиш е изследвал и обикновения въздух, за да определи състава на атмосферата. Карл Шееле (1742 – 1786), един от откривателите на кислорода и азота, вече е определил, че въздухът е смес от двата елемента. Кавендиш е установил, че пропорцията е 20,83 % кислород и 79,17 % азот, като всичко друго се смята за примеси.
Кавендиш е изследвал и обикновения въздух, за да определи състава на атмосферата. Карл Шееле (1742 – 1786), един от откривателите на кислорода и азота, вече е определил, че въздухът е смес от двата елемента. Кавендиш е установил, че пропорцията е 20,83 % кислород и 79,17 % азот, като всичко друго се смята за примеси.